Historia y descubrimiento de LAL
En 1956 Bang descubrió una enfermedad bacteriana en el cangrejo de herradura, la cual producía coagulación de la sangre del cangrejo de herradura. En 1964, 1968 Levin y Bang elucidaron los mecanismos de coagulación y demostraron que los componentes que se coagulaban se encontraban en la sangre del cangrejo de herradura. Llegando a la conclusión que la coagulación era el producto de una cadena enzimática producida por la presencia de las endotoxinas bacterianas en la sangre del cangrejo.
En una noticia del 12 de Enero de 1973, la FDA anunció que el Lisado de Amebocitos de Lymulus (LAL), derivado de las células sanguíneas (amebocitos) del cangrejo de herradura, (Limulus Polyphemus) es un producto biológico, el cual es usado como indicador sensitivo de la presencia de endotoxinas bacterianas (pirógenos) causantes de fiebre, shock, e incluso muerte en humanos y animales. La prueba LAL es más rápida, económica, y requiere menos volumen del producto que lo que requiere la prueba de pirógenos en conejos; sin mencionar que el procedimiento de trabajo es menos laborioso que la prueba de pirógeno en conejos; por estas razones, usando los reactivos para la prueba LAL se pueden realizar muchas pruebas en un día.
Endotoxinas
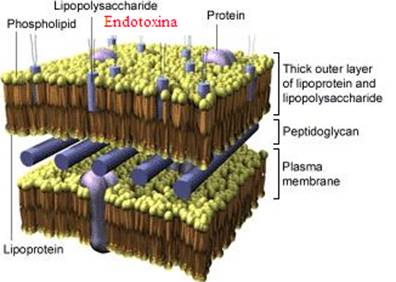
Las endotoxinas son compuestos pirogénicos únicos de bacterias gram negativas. Dichas endotoxinas son componentes estructurales de la pared celular externa de las bacterias gram negativas. Las endotoxinas son liberadas al medio ambiente cuando las bacterias se dividen o cuando mueren.
Aplicaciones de la prueba LAL
Entre las aplicaciones que tiene esta prueba figuran:
- Prueba de endotoxinas en drogas parenterales.
- Prueba de endotoxinas en artículos médicos.
- Pruebas de productos biológicos (naturales y biotecnológicos).
- Prueba de medios de cultivo de tejidos.
- Prueba de agua de diálisis.
- Prueba de agua de alta pureza.
- Prueba de alimentos.
Guía de Lisado FDA de Amebocitos
